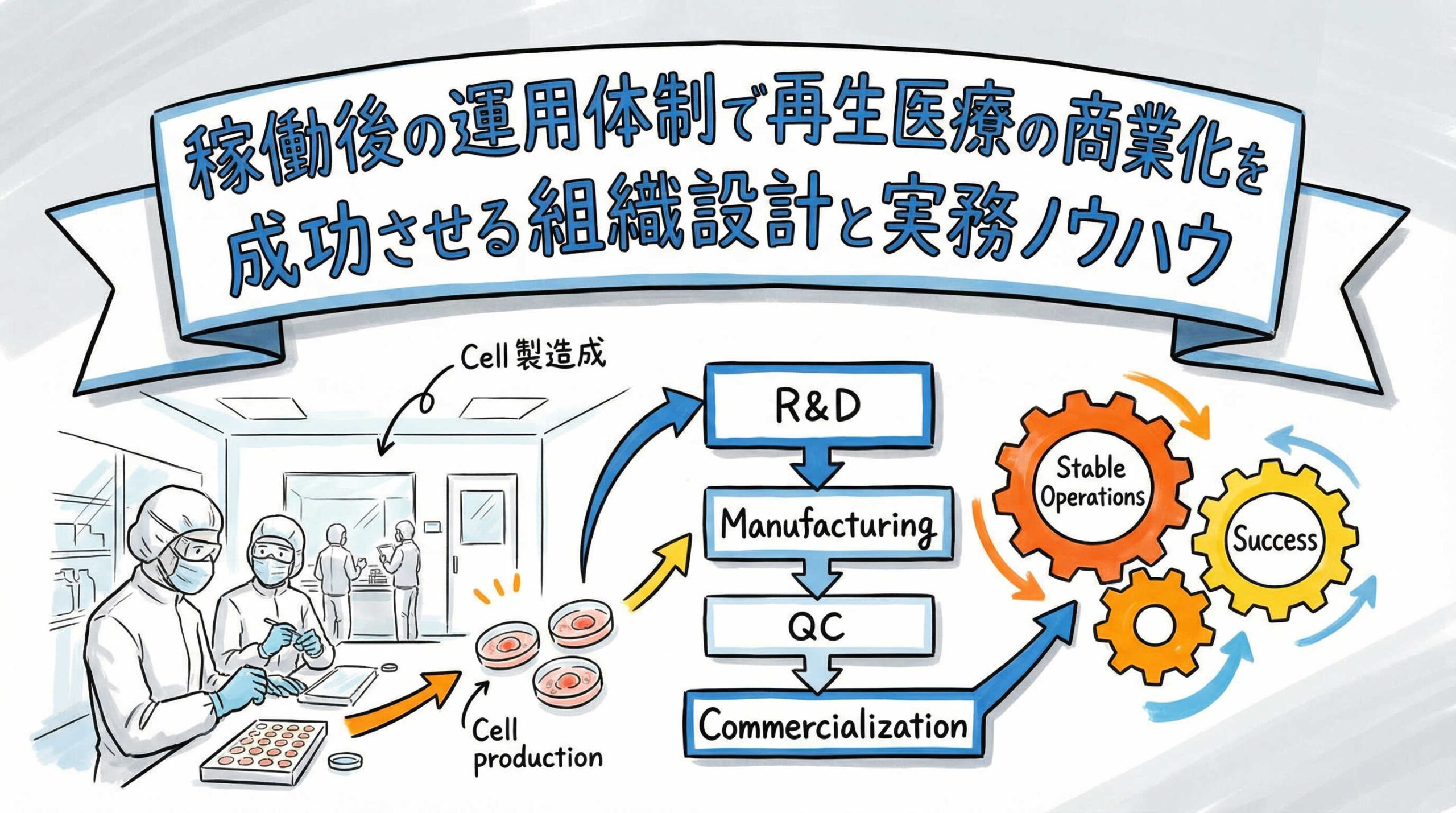
細胞培養加工施設(CPC)の建設や設備導入といったハード面の計画が進む中で、多くのプロジェクト責任者様が次に直面するのが「稼働後の運用体制」というソフト面の課題ではないでしょうか。GCTP省令に適合した製造管理・品質管理体制を構築し、かつ商業ベースで採算の取れる効率的な運用を維持することは、再生医療事業の成功における最大のハードルと言っても過言ではありません。
本記事では、再生医療の商業化を見据えた運用体制の構築について、組織図の設計からSOP(標準作業手順書)の整備、教育訓練、そして外部リソースの活用まで、実務的な観点から詳しく解説します。査察をクリアし、安定した製造ラインを確立するための具体的なノウハウを、ぜひ貴社の計画にお役立てください。
再生医療の商業化における「稼働後の運用体制」の結論

再生医療等製品の事業化において、施設という「箱」が完成しても、それを動かす「人」と「仕組み」が整っていなければ製造は開始できません。稼働後の運用体制を検討する上で、まず押さえておくべき重要な結論について解説します。
GCTP省令への適合と事業採算性の両立が必須
再生医療事業を成功させるためには、GCTP(Good Gene, Cellular, and Tissue-based Products Manufacturing Practice)省令への厳格な適合と、事業としての採算性を両立させることが不可欠です。
規制要件を満たすことは大前提ですが、過剰な管理体制や非効率な手順は製造コストを押し上げ、製品価格に跳ね返ります。一方で、コスト削減を優先してコンプライアンスをおろそかにすれば、回収命令や業務停止といった致命的なリスクを招きかねません。
したがって、「法規制が求める品質保証レベルをクリアしつつ、無駄のないスリムな運用体制」を設計することが、稼働後の運用における最大のゴールとなります。
ハード(施設)完成前からソフト(組織・手順)の構築を始めるべき理由
運用体制の構築は、施設の設計・建設と並行して、あるいはそれよりも早い段階から着手する必要があります。なぜなら、ハードウェア(施設・設備)の仕様は、ソフトウェア(製造プロセス・人の動き・清掃手順など)と密接に連動しているからです。
また、GCTPに準拠したSOP(標準作業手順書)の作成や、製造・品質部門の人員確保、そして彼らへの教育訓練には、想像以上の時間を要します。施設が完成してから運用ルールを決め始めたのでは、製造業許可申請や適合性調査のスケジュールに間に合わず、商業化のタイミングを逸してしまうリスクが高まるでしょう。
- SOP作成期間: 数ヶ月〜半年以上
- 要員採用・教育: 半年〜1年
- 模擬製造・バリデーション: 数ヶ月
このように、ソフト面の構築には長いリードタイムが必要であることを認識し、早期にアクションを起こすことが肝要です。
稼働後の運用体制構築が重要視される背景

なぜ今、多くの企業が「稼働後の運用体制」の構築に注力しているのでしょうか。単にルールを守るためだけではなく、事業の継続性やリスク管理の観点から、その重要性が高まっている背景を掘り下げてみましょう。
規制当局による実地査察・適合性調査への対応
再生医療等製品製造業許可の取得や更新、あるいは製品承認時には、PMDA(医薬品医療機器総合機構)や都道府県による実地査察(適合性調査)が行われます。この調査では、施設設備の状態だけでなく、運用体制が適切に機能しているかが厳しく問われます。
- 組織の責任体制が明確か
- 手順書通りに作業が行われているか
- 記録が正確に残されているか
これらは、日々の運用の中で培われるものであり、査察直前に取り繕えるものではありません。確実な許認可取得のためには、実地査察に耐えうる強固な運用体制を、日常的に維持しておく必要があります。
商業生産フェーズにおける製造コスト管理と効率化
研究開発フェーズから商業生産フェーズに移行すると、コスト管理の重要性が一気に増します。商業生産では、一定の品質を保ちながら、継続的に製品を市場へ供給しなければなりません。
運用体制が非効率だと、作業ミスによる廃棄ロス、過剰な人員配置による人件費の増大、トラブル対応による稼働停止などが発生し、製造原価を圧迫します。稼働後の運用体制を最適化することは、製造コスト(CoG:Cost of Goods)を適正化し、事業の収益性を確保するための経営課題そのものと言えるでしょう。
ヒューマンエラーの防止と品質リスクの低減
再生医療等製品の製造は、自動化が進んでいるとはいえ、依然として手作業に依存する工程が多く存在します。そのため、ヒューマンエラーのリスクを完全に排除することは困難です。
しかし、適切な運用体制があれば、エラーの発生を未然に防いだり、発生したとしても早期に発見し影響を最小限に留めたりすることが可能です。
- ダブルチェック体制の確立
- 誤認を防ぐ識別管理
- 疲労やストレスを考慮したシフト管理
これらを組織的に組み込むことで、患者様の安全に関わる品質リスクを低減させることが、運用体制構築の大きな目的の一つです。
GCTP適合に向けた組織体制と人員配置の具体例

GCTP省令に適合するためには、どのような組織構造を作り、誰を配置すればよいのでしょうか。ここでは、具体的な役割分担や人員配置の考え方について、実務的な視点で解説します。
製造管理者の要件と業務を統括する役割
再生医療等製品の製造所には、「製造管理者」の設置が義務付けられています。製造管理者は、製造所の業務を統括し、従業員を監督し、構造設備や製品の管理を行う極めて重要なポジションです。
法令上の要件(医師、歯科医師、薬剤師、獣医師、または厚生労働大臣が認めた者など)を満たすことはもちろんですが、実務的には以下のような能力が求められます。
- GCTP省令の深い理解と遵守
- トラブル発生時の的確な判断力
- 製造部門と品質部門を統率するリーダーシップ
単なる名義貸しではなく、現場に常駐し、実質的な管理を行える人物を配置することが、適正な運用の第一歩です。
製造部門と品質部門(QA/QC)の独立性と相互連携
GCTP運用において最も重要な原則の一つが、製造部門と品質部門(QA:品質保証 / QC:品質管理)の独立性です。製造部門は「製品を作ること」に責任を持ち、品質部門は「製品の品質を確認し、出荷の可否を判定すること」に責任を持ちます。
もし製造部門が品質判定も兼ねてしまうと、納期やコストの圧力を受けて、不適合品を合格させてしまうリスクが生じます。そのため、組織図上でも指揮命令系統を明確に分け、品質部門が製造部門に対して独立した権限を持つ体制(牽制機能)を構築しなければなりません。
運用に必要な人員数の算出とバックアップ体制の検討
CPCの運用には、製造担当者や品質担当者だけでなく、施設管理、文書管理、教育訓練などを担当する人員も必要です。必要な人員数を算出する際は、以下の要素を考慮しましょう。
- 製造ロット数と工程所要時間
- 無菌操作における更衣や清掃の時間
- 記録作成やダブルチェックの手間
また、ギリギリの人員配置は避けるべきです。担当者の急な病欠や退職、あるいは産休・育休などが発生しても業務が回るよう、多能工化(マルチスキル化)を進めたり、予備の人員を確保したりするバックアップ体制の検討が、安定稼働には不可欠です。
安定稼働を支える業務フローと文書管理システム(SOP)

組織ができても、具体的な「動き方」が決まっていなければ現場は混乱します。安定稼働を支えるのは、体系化された業務フローと、それを明文化した文書管理システムです。
製造管理基準書・品質管理基準書等の体系的な整備
GCTPでは、製造管理基準書、品質管理基準書、衛生管理基準書といった「三大基準書」をはじめ、多くの手順書の作成が求められます。これらはバラバラに存在するのではなく、体系的に整理されている必要があります。
- 製品標準書: 製品ごとの規格や製造方法のマスター
- 基準書: 業務全体の方針やルール(上位文書)
- 手順書(SOP): 具体的な作業手順(下位文書)
- 記録様式: 作業結果を残すフォーマット
このように文書の階層構造(ドキュメントピラミッド)を意識し、誰が読んでも同じ作業ができるよう、具体的かつ明確に記述することが重要です。
逸脱発生時の対応フローと是正・予防措置(CAPA)
製造過程では、手順書通りにいかない予期せぬ事態(逸脱)が必ず発生します。重要なのは、逸脱を隠すことではなく、速やかに報告し適切に対処するフローを確立することです。
- 逸脱報告: 発生の検知と初期対応
- 影響評価: 製品品質への影響範囲の特定
- 原因究明: なぜ起きたのか(Root Cause Analysis)
- CAPA(是正処置・予防処置): 再発防止策の実施
このCAPAプロセスを確実に回すことで、組織は失敗から学び、運用体制をより強固なものへと進化させることができます。
変更管理(Change Control)の適切な運用手順
稼働後、製造手順や設備、原材料などを変更したい場面が出てきます。しかし、思いつきで変更を行うことは厳禁です。変更が製品の品質に悪影響を与えないか、事前に検証する必要があります。
これを管理するのが「変更管理」です。変更の提案、リスク評価、承認、実施、そして変更後の評価という一連の手順をSOPとして定め、承認なしに変更が行われないよう厳格に運用します。適切な変更管理は、恒常的な品質維持の要となります。
データインテグリティ(DI)を考慮した記録管理
近年、規制当局が特に注視しているのがデータインテグリティ(DI:データの完全性)です。手書き記録であれ電子データであれ、データが正確で、改ざんされておらず、信頼できるものであることが求められます。
- Attributable(誰が)
- Legible(読みやすく)
- Contemporaneous(同時的記録)
- Original(原本)
- Accurate(正確)
これらALCOA+の原則に基づき、修正液を使わない訂正方法の徹底や、電子システムのアクセス権限管理など、データの信頼性を担保する仕組みを運用フローに組み込む必要があります。
稼働後の品質維持に必要な教育訓練と施設管理

運用体制は一度作って終わりではありません。日々の活動を通じて品質レベルを維持・向上させていくためには、継続的な教育と徹底した施設管理が求められます。
無菌操作・GCTPに関する継続的な教育訓練計画と評価
再生医療の製造において、作業者の手技は品質に直結します。そのため、初期教育だけでなく、定期的な教育訓練が欠かせません。
- 座学: GCTP省令、衛生管理、微生物学の基礎など
- 実技: 無菌操作、ガウンテクニック、培地交換など
これらを計画的に実施し、単に「受けた」だけでなく「理解し、習得した」ことを評価・認定する制度を設けることが望ましいでしょう。また、逸脱が発生した際には、再教育を行い、スキルレベルを再確認するプロセスも重要です。
清浄度区分に応じた環境モニタリングの実施体制
CPC内の清浄度は、製品の汚染リスクを管理する上で最も重要な指標の一つです。グレードA、B、C、Dといった清浄度区分に応じ、微粒子や微生物のモニタリングを定期的に実施します。
- モニタリング頻度: 作業時、非作業時など
- 測定ポイント: リスクの高い場所を選定
- アラート/アクションレベル: 異常の予兆を捉える基準値
これらのデータをトレンド分析し、環境が悪化する兆候があれば、清掃方法の見直しやフィルタ交換などの対策を講じ、常に管理された状態を維持します。
製造設備・機器の保守点検と校正(キャリブレーション)
安全キャビネット、CO2インキュベーター、フリーザーなどの製造機器は、常に正常に動作していなければなりません。定期的な保守点検(メンテナンス)はもちろんのこと、計測機器が正しい値を示しているかを確認する「校正(キャリブレーション)」も重要です。
機器ごとに管理責任者を定め、点検計画を策定し、実施記録を残します。また、バリデーションされた状態(適格性)が維持されていることを定期的に確認することで、ハードウェア起因のトラブルを未然に防ぐことができます。
運用体制の構築・維持における外部リソースの活用検討

ここまで解説してきた運用体制を、すべて自社のリソースだけで構築・維持するのは容易ではありません。事業戦略に応じて、外部の専門家やパートナーを活用することも有力な選択肢です。
自社単独運用におけるリソース不足とコンプライアンスリスク
特に新規参入企業やベンチャー企業の場合、GCTPに精通した経験豊富な人材を社内だけで確保するのは困難な場合があります。無理に自社単独での運用にこだわると、以下のようなリスクに直面する可能性があります。
- 解釈の誤り: 規制要件を読み違え、不適切な運用をしてしまう
- ノウハウ不足: トラブル発生時に適切な対応ができず、復旧が遅れる
- リソース枯渇: 特定の担当者に業務が集中し、組織が疲弊する
結果として、コンプライアンス違反や事業の停滞を招く恐れがあるため、自社の実力を客観的に評価することが大切です。
運用支援コンサルティングや外部委託導入の判断基準
不足するリソースを補うためには、運用支援コンサルティングの導入や、製造業務の一部または全部をCDMO(医薬品製造開発受託機関)へ委託することを検討しましょう。
- コンサルティング: 運用体制の設計支援、模擬査察、SOP作成支援など、自社にノウハウを蓄積したい場合に有効。
- CDMO: 製造そのものをプロに任せることで、設備投資や固定費を抑制し、開発やマーケティングにリソースを集中させたい場合に有効。
コスト、スピード、社内に残すべき技術、そして将来の事業展開を総合的に判断し、最適なパートナーシップを選択してください。
まとめ

再生医療事業における「稼働後の運用体制」は、施設の建設と同じくらい、あるいはそれ以上に重要な成功因子です。GCTP省令への適合はもちろん、採算性の確保、リスク管理、そして人材育成までを含めた包括的な視点が必要となります。
ハードウェアが完成してから慌てるのではなく、早期から組織体制や業務フロー(SOP)の構築に着手し、教育訓練を徹底することで、スムーズな商業化が可能となります。また、必要に応じて外部リソースを賢く活用することも、安定稼働への近道です。
確固たる運用体制を築くことは、規制当局への信頼だけでなく、何よりも患者様への安全な製品供給を約束することに他なりません。本記事が、貴社の持続可能な事業運営の一助となれば幸いです。
稼働後の運用体制についてよくある質問

再生医療の稼働後の運用体制に関して、よく寄せられる質問をまとめました。